THP-1細胞來源的巨噬細胞,具備人源背景、均一性好、培養簡便等優點,被廣泛用于炎癥機制、腫瘤免疫、病原感染及免疫藥物篩選研究。這份精簡提煉的THP-1細胞誘導巨噬細胞方案,帶你精準避坑,誘導極化一步到位!
THP-1細胞
源自急性單核細胞白血病患者外周血的單核細胞,是一種懸浮生長的細胞系。
培養體系
RPMI1640培養基+10%胎牛血清+1%雙抗+0.1%β-巰基乙醇。
形態特征
懸浮的透亮的體積較小的圓形細胞,少數聚團,飽滿且輪廓清晰;
在偏酸性環境中生長較快,即當培養基稍微變黃(呈橘紅色)時。
向M0巨噬細胞分化
PMA誘導方法
-
收集狀態良好的THP-1細胞并進行細胞計數; -
調整細胞密度為5×105個/mL,接種至六孔板,每孔加入2 mL細胞懸液; -
向孔中加入終濃度為100 ng/mL的PMA孵育24-48 h。
誘導成功的標志
形態特征:THP-1細胞用PMA誘導后,由懸浮式生長變成貼壁生長,由圓形變成不規則形態;細胞體積增大,細胞核增大明顯,可見大量明顯細胞器,胞膜周圍可見少量突起。
表型特征:F4/80、CD11b雙陽可作為鑒定巨噬細胞成熟的標志蛋白。
向M1/M2巨噬細胞極化
-
去除PMA后,用RPMI 1640完全培養基靜息24h后:
-
M1極化:加入100 ng/mL的LPS和20 ng/mL的 IFN-γ(Cat#C014)培養24-48 h;
-
M2極化:加入20 ng/mL的IL-4(Cat#CX03)和20 ng/mL 的IL-13(Cat#CC89)培養48-72 h;
-
細胞鑒定:M1巨噬細胞上調表達CD86,M2巨噬細胞上調表達CD206。
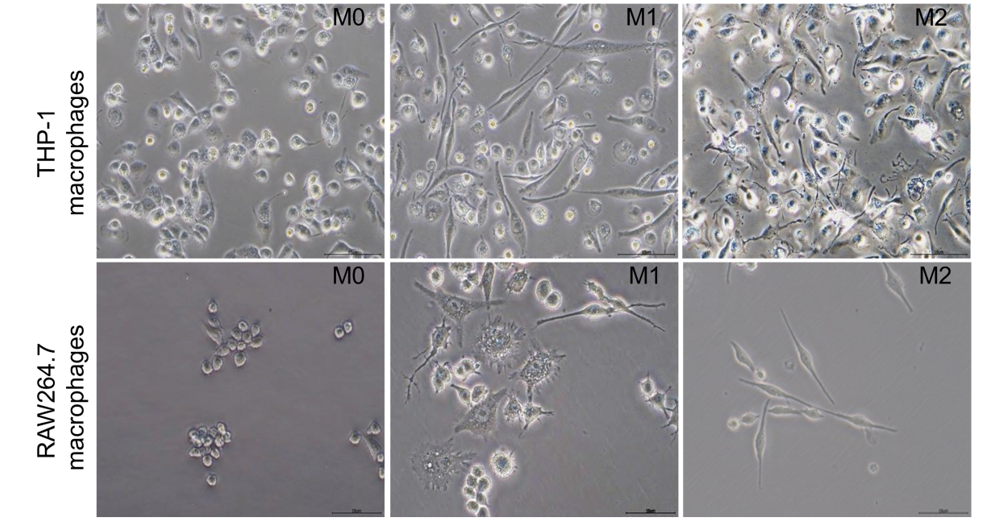
THP-1來源巨噬細胞形態[1]
THP-1細胞極化Q&A
Q1:THP-1細胞培養基中必須要加β巰基乙醇嗎?
β-巰基乙醇是一種常用的培養補充劑,有抗氧化的作用,可減少氧化應激對THP-1細胞的影響。實驗過程可以根據具體的培養時間以及細胞密度而定,如果細胞培養在48 h內可以不用加β-巰基乙醇,如果培養周期較長,細胞密度過大但需要維持細胞狀態時,可適當增加β-巰基乙醇的比例。
Q2:THP-1細胞極化M1和M2時是否需要靜息培養?
一般而言,靜息培養對THP-1細胞極化M1影響不大,THP-1細胞極化M2時靜息培養效果會更明顯。
Q3:THP-1細胞誘導M1和M2時培養基不用加PMA嗎?
THP-1細胞誘導M1和M2時需要先加入PMA誘導極化為M0后,再進行后續M1和M2的培養,后續誘導M1和M2分化時,不需要加入PMA,加入PMA長期作用會促使細胞發生凋亡。
Q4:THP-1細胞誘導M2時,CD206表達低,僅為10%左右怎么辦?
可以進行優化。降低PMA濃度(如100 ng/mL→50 ng/mL);延長靜息時間至48h;M2極化延長至48-72h。
更多巨噬細胞來源,如小鼠骨髓(BMDM)、PBMC、RAW264.7來源等,掃碼免費獲取完整版《巨噬細胞誘導實驗手冊》

近岸蛋白可提供高分引用文獻的IFN gamma,IL-4,IL-13等細胞因子產品,高活性,低內毒素,助力體外巨噬細胞培養。
產品推薦—巨噬細胞培養因子
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
參考文獻
[1] Li P, Hao Z, Wu J, et al. Comparative Proteomic Analysis of Polarized Human THP-1 and Mouse RAW264.7 Macrophages. Front Immunol. 2021;12:700009. doi:10.3389/fimmu.2021.700009.
